结构化学基础贰
约定:本文用加粗标记定义或概念,实验名称由斜体标注。本文中部分图片为网图,侵删。
1. 元素周期律
在元素周期表中,原子电核电荷数、原子量、半径、电离能、电子亲和能、电负性等呈现周期变化,而这些原子的特征被称作原子参数。
1.1 原子轨道半径
原子轨道半径指的是最外层轨道分布图主峰到中心的距离。差不多可以理解为,最外层轨道到原子核的距离。
- 同周期,核电荷数增加,引力增大,原子半径减小。(➡️小)
- 同一族,主量子数增加,电子层数变多,原子半径增大。(⬇️大)
- 电子层数的影响比核电荷数引力的影响大。
- 例外: 、 与 族元素,半径会反而变大(因为出现了电子的全充满)。
微粒半径大小取决于:
- 电子层数(优先级最高);
- 核电荷数(优先);
- 电子斥力/电子数。
镧系中原子半径缓慢减小,称作镧系收缩。
镧系收缩造成的影响:第二、第三过渡系的元素性质相近、分离困难。
第二过渡系和第三过渡系是指元素周期表中的两个副族。 第二过渡系是第5周期的副族,包括镧系元素和锕系元素。 第三过渡系是第6周期的副族,包括镧系元素和锕系元素。
1.1.1 共价半径
当两个原子间产生共价键时,就会有共价半径。
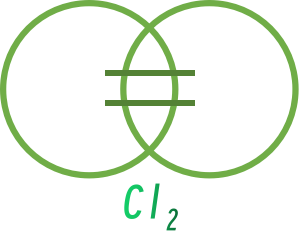
1.1.2 金属半径
对于金属原子,相互之间也会产生一个作用力,称作金属半径。
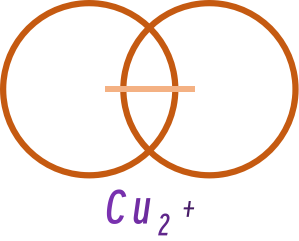
1.1.3 范德华半径
范德华力是另一种分子间的作用力,具体地,有三个细分的力,后面会细讲。
对角线规则:一个元素,右边一格再下面一格的元素,这两个元素的原子半径相似、性质也相似。
1.2 电离能
电离能的大小可以用来衡量原子失去电子的难易,也可以用来判断原子失去电子的数目和形成的阳离子所带的电荷
1.2.1 第一电离能
第一电离能指的是基态的气态原子失去最外层的一个电子所需的能量。
1.2.2 第二电离能
指已经失去了一个电子,再失去第二个电子时所需的能量。
影响电离能的因素:
- 距离原子中心的半径(主要因素),半径越大,电离能越小;
- 电子半满/全满的情况,会使电离能增加。
常见规律:
- 的元素,其最高价态等于它的族数。
- 金属元素的电离能一般低于非金属元素。
反常现象:
- 系收缩,使 ;
- 系收缩,使 , 。
1.3 电子亲和能
原子的电子亲和能是指一个气态原子得到一个电子形成气态负离子所放出的能量,常以符号 表示。
注意,电子亲和能有正有负。正值表示放出能量,负值表示吸收能量。
第一电子亲和能通常为正值,放热;而第二、第三电子亲和能通常为负值,吸热。
第一电子亲和能在元素周期表中的规律:
- 向➡️,第一亲和能增大;
- 向⬇️,第一亲和能变小。
电子亲和能反映了原子获取电子的能力。元素原子的第一电子亲和能的代数值愈大,该元素的一个基态的气态原子得到一个电子形成 价气态阴离子时所放出的能量越多,元素原子得到电子的倾向愈大,元素的非金属性也愈强。
1.4 电负性
之前的电离能、电子亲和能中都有离子的出现,都是原子变成了离子。而本节所说的电负性是用来衡量分子中的原子相互吸引成键的能力。
要点:
- 规定氟的电负性为 。
- 电负性可以用来衡量金属性和非金属性的强弱。
- 如果吸引电子的能力较强,则显示电负性;如果吸引电子的趋势较弱,则显示电正性。
- 电离能、亲和能,针对的是(气体)离子化合物;而电负性讨论的是共价化合物。
绝对电负性计算公式:
其中, 为电离能, 为电子亲和能。我们可以将它们的平均值看作绝对电负性。上式中均以 作为单位。
2. 核化学
2.1 放射性衰变
- 衰变: (左移两格)
- 衰变: (左移y一格)
- 衰变:
2.2 放射系
- 铀系
- 钍系
- 锕系
是放射衰变的终点,因为它最稳定。
2.3 核化学方程式
原则:质量数(在左上角)和原子序数(在左下角),左右两边加和相等。
2.4 半衰期
对特定元素来说是定值,符号为 。
半衰期的计算:假定初始浓度为 ,过了 时间后为 。则有:
即:
的半衰期为 ( 年)。通过测定其含量可估算其出现年代。
2.5 结合能
核素间的平均结合能:核素之间靠核力结合成原子核。结合时会损失的能量 称作结合能。
2.6 核裂变与核聚变
有核裂变与核聚变两种形式。
补充,分区的概念:最后一个电子填在那个轨道就是什么区( 区, 区……)。
支持与分享
如果这篇文章对你有帮助,欢迎分享给更多人或赞助支持!
 无穷大?
无穷大? 











